Kryštalizácia je základnou metódou v chémii, ktorá umožňuje získať čisté tuhé látky. Ide o proces prechodu látky z amorfného stavu (plynného, taveniny alebo roztoku) do usporiadaného kryštalického stavu. Aby kryštalizácia z roztoku úspešne prebehla, musí byť roztok presýtený, čo znamená, že obsahuje viac rozpustenej látky, ako by sa za danej teploty bežne rozpustilo.
Princípy kryštalizácie z roztokov
Proces vylučovania kryštálov z roztoku je možné iniciovať niekoľkými spôsobmi:
- Odparením rozpúšťadla: Postupným odparovaním rozpúšťadla sa zvyšuje koncentrácia rozpustenej látky, až kým roztok nedosiahne bod presýtenia a nezačnú sa tvoriť kryštály.
- Ochladením roztoku nasýteného za horúca: Rozpustnosť mnohých látok klesá so znižujúcou sa teplotou. Ochladením nasýteného roztoku sa zníži jeho schopnosť rozpúšťať látku, čo vedie k presýteniu a následnej kryštalizácii.
- Ovplyvnením rozpustnosti: Rozpustnosť látky je závislá od rôznych faktorov, ako je chemická štruktúra látky, typ rozpúšťadla a teplota. Zmenou týchto podmienok, napríklad pridaním iného rozpúšťadla, v ktorom je kryštalizujúca látka menej rozpustná, je možné vyvolať kryštalizáciu.
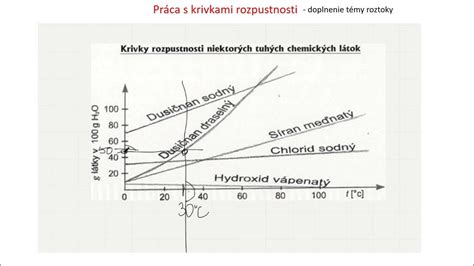
Teplotná závislosť koncentrácie nasýteného roztoku sa opisuje pomocou krivky rozpustnosti.
Metódy kryštalizácie a ich vplyv na veľkosť kryštálov
Spôsob a rýchlosť kryštalizácie majú zásadný vplyv na veľkosť výsledných kryštálov. Existuje niekoľko základných metód:
Voľná kryštalizácia
Pri voľnej kryštalizácii sa nechá nasýtený roztok pomaly ochladzovať v pokoji. V takomto prostredí vzniká menej kryštalizačných centier, čo vedie k tvorbe menšieho počtu, ale zato väčších kryštálov. Je to ideálna metóda pre získanie esteticky pôsobivých, veľkých kryštálov.
Prerušená (nútená) kryštalizácia
Táto metóda spočíva v prudkom ochladzovaní a súčasnom miešaní nasýteného roztoku. Miešanie podporuje vznik veľkého množstva kryštalizačných centier, čoho výsledkom je tvorba jemne kryštalickej látky, teda mnohých malých kryštálikov.
Kryštalizácia zmenou rozpúšťadla
Využíva sa rozdielna rozpustnosť látky v rôznych rozpúšťadlách. Pridaním rozpúšťadla, ktoré sa mieša s pôvodným rozpúšťadlom, ale v ktorom je kryštalizujúca látka horšie rozpustná, dôjde k jej vylúčeniu vo forme kryštálikov. Veľkosť kryštálov závisí od toho, či sa rozpúšťadlo pridáva naraz za miešania, alebo postupne bez miešania.
Kryštalizácia pridaním látky so spoločným iónom
Táto metóda je obzvlášť účinná pri kryštalizácii solí. Pridaním inej látky, ktorá obsahuje spoločný ión s kryštalizujúcou látkou, sa zníži jej rozpustnosť v roztoku, čím sa urýchli proces kryštalizácie a často sa zväčší množstvo vytvorených kryštálikov.
Praktická realizácia kryštalizácie modrej skalice
Pre rýchlu kryštalizáciu modrej skalice (pentahydrát síranu meďnatého) je možné použiť rôzne prístupy:
Príprava polykryštalickej vzorky modrej skalice
Pre tento postup potrebujete pentahydrát síranu meďnatého (kúpiteľný v záhradkárstvach alebo špecializovaných predajniach chemikálií), zavárací pohár (cca 720 ml) a kameň strednej veľkosti.
- Do 200 ml vody priveďte do varu a rozpustite v nej 124 g pentahydrátu síranu meďnatého. Miešajte, kým sa všetok síran nerozpustí.
- Do zaváracieho pohára vložte vybraný kameň.
- Horúci roztok modrej skalice prelejte do pohára tak, aby kameň bol úplne ponorený.
- Pohár umiestnite na stabilné miesto, napríklad na okenný parapet.
TIP: Pre najlepšie výsledky odporúčame použiť destilovanú vodu, nakoľko voda z vodovodu obsahuje ióny, ktoré môžu ovplyvniť rast kryštálov.
Počas ochladzovania roztoku s kameňom sa začnú tvoriť kryštály. Je dôležité nádobu počas tohto procesu nechať v pokoji, aby sa nenarušil rast kryštálov. Po dosiahnutí požadovanej veľkosti kryštálov roztok opatrne vylejte a vzorku vyberte.

Oddeľovanie nečistôt kryštalizáciou modrej skalice
Ak chcete získať čistú modrú skalicu z materiálu s nerozpustnými prímesami (napr. drevené piliny, krieda, piesok), postupujte nasledovne:
- V kadičke zohrejte 50 cm³ vody na teplotu približne 70 °C.
- Do zohriatej vody postupne pridávajte znečistenú modrú skalicu za stáleho miešania, až kým sa prestane rozpúšťať.
- Zmes zohrievajte takmer do varu za občasného miešania.
- Horúcu zmes opatrne prefiltrujte cez filtračný papier do kužeľovej banky. Pri filtrácii zostanú nerozpustné nečistoty na filtračnom papieri.
- Filtrát v kužeľovej banke ochlaďte pod tečúcou vodou, pričom roztok jemne miešajte krúživým pohybom banky po dobu asi 10 minút.
- Vylúčené kryštály oddeľte od zvyškového roztoku filtráciou.
Týmto postupom sa efektívne oddelia nerozpustné nečistoty a získa sa čistejší produkt.

Postup kryštalizácie pre rôzne metódy
Pre porovnanie rôznych metód kryštalizácie môžeme použiť nasýtený roztok modrej skalice alebo chloridu sodného. Pripraví sa nasýtený roztok danej látky pri vyššej teplote (napr. odparením rozpúšťadla alebo rozpustením maximálneho možného množstva látky za tepla). Tento roztok sa potom rozdelí na časti a aplikujú sa na ne rôzne metódy kryštalizácie:
- Voľná kryštalizácia: Jedna časť roztoku sa nechá v pokoji kryštalizovať.
- Prerušená kryštalizácia: Druhá časť sa prudko ochladí a mieša.
- Kryštalizácia zmenou rozpúšťadla: Do tretej časti sa pridá rozpúšťadlo, v ktorom kryštalizujúca látka nie je rozpustná.
- Kryštalizácia pridaním látky so spoločným iónom: Pri kryštalizácii chloridu sodného sa štvrtá časť obohatí o látku so spoločným iónom (napr. NaCl sa pridá do roztoku obsahujúceho ióny Na+ alebo Cl-).
Porovnaním veľkosti a množstva kryštálov získaných jednotlivými metódami je možné demonštrovať vplyv spôsobu kryštalizácie na výsledok.
Faktory ovplyvňujúce rýchlosť chemických reakcií
Rýchlosť chemických reakcií, vrátane kryštalizácie, je ovplyvnená viacerými faktormi:
- Koncentrácia reaktantov: Vyššia koncentrácia zvyšuje pravdepodobnosť zrážok medzi časticami a tým aj rýchlosť reakcie.
- Teplota: Vyššia teplota dodáva časticiam viac kinetickej energie, čo vedie k častejším a účinnejším zrážkam a teda k rýchlejšej reakcii.
- Veľkosť povrchu reaktantov: Väčší povrch umožňuje intenzívnejšiu interakciu medzi reaktantmi, čo urýchľuje reakciu.
Dôležité upozornenia pri práci s modrou skalicou
Pri manipulácii s modrou skalicou je potrebné dbať na jej ekologickú a zdravotnú nebezpečnosť:
- Ochrana životného prostredia: Zvyšné roztoky modrej skalice nevylievajte do odpadu ani do prírody. Zbierajte ich do osobitnej nádoby.
- Ochrana pokožky: Modrá skalica môže dráždiť pokožku, preto sa odporúča používať ochranné rukavice.
- Uchovávanie: Modrá skalica obsahuje kryštálovú vodu, ktorá sa pôsobením tepla uvoľňuje (dehydratácia). Vzorky uchovávajte na chladnom mieste. Pre dlhodobú ochranu je možné kryštály natrieť bezfarebným lakom na nechty.
- Čistenie: V prípade potreby očistenia vzoriek sa nepoužíva voda, ale skôr utierka alebo štetec.
tags: #rychla #krystalizacia #modrej #skalice #aparatura