Vo svete okolo nás sa látky vyskytujú v rôznych skupenstvách. Poznáme štyri základné skupenstvá: pevné, kvapalné, plynné a plazma. Na základnej škole sa zvyčajne zameriavame na prvé tri - pevné, kvapalné a plynné, pričom vlastnosti látok v týchto skupenstvách sú detailne rozoberané v základoch fyziky.
Tento príspevok sa však bude venovať fascinujúcim procesom premeny skupenstiev. Schéma nižšie nám ukazuje, ako sa tieto premeny nazývajú.
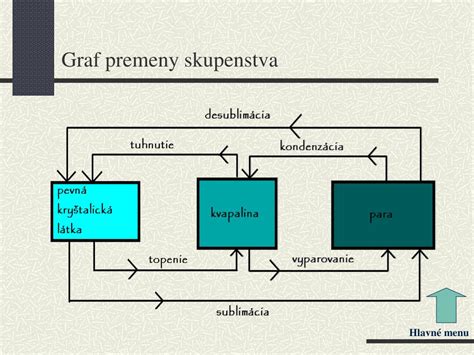
Vyparovanie a var
Vyparovanie je proces, pri ktorom sa kvapalina mení na plyn. Tento jav prebieha za akýchkoľvek podmienok, bez ohľadu na teplotu či tlak. Rýchlosť vyparovania je ovplyvnená niekoľkými faktormi: teplotou kvapaliny, veľkosťou jej povrchu a intenzitou odstraňovania pár z jej okolia.
Kvapalina sa môže vyparovať buď len zo svojho povrchu, alebo v celom objeme. Intenzívnejšou formou vyparovania je var. Pri vare sa kvapalina premieňa na plyn v celom svojom objeme, nie len z povrchu. Navonok sa to prejavuje charakteristickým "bublaním", teda tvorbou bubliniek.
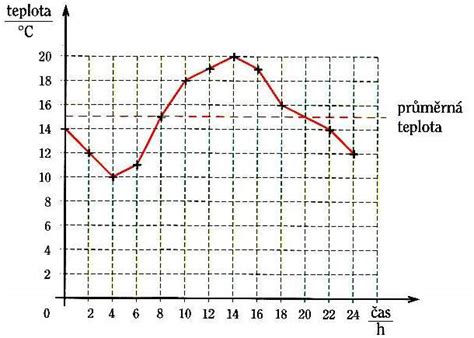
Počas varu sa teplota sústavy nemení, aj keď na ňu naďalej dodávame teplo. Všetka dodaná energia sa spotrebúva na proces odparovania, ktorý je energeticky náročný. Na grafe závislosti teploty od dodaného tepla sa tento jav prejaví ako zlom - teplota najprv stúpa, potom pri dosiahnutí teploty varu zostáva konštantná, až kým sa všetka kvapalina nepremení na plyn.
Teplota varu nie je konštantná, ale závisí od atmosférického tlaku. Zvýšenie tlaku vedie k zvýšeniu teploty varu, avšak táto závislosť nie je priamo úmerná. Atmosférický tlak je tlak vyvolaný plynným obalom Zeme, atmosférou, ktorá siaha stovky kilometrov nad jej povrch.
Ako je možné dosiahnuť vyššiu teplotu varu, ak voda pri normálnom tlaku vrie pri 100°C? Zvýšením tlaku. Na tomto princípe funguje tlakový hrniec (Papinov hrniec). Jeho tesne uzavretá pokrievka zabraňuje úniku pary, čím sa zvyšuje tlak nad vodou a tým aj jej teplota varu.
Kondenzácia
Kondenzácia, nazývaná aj skvapalňovanie alebo zrážanie, je opačný proces k vyparovaniu - premena plynu na kvapalinu. Na rozdiel od vyparovania, kondenzácia neprebieha za každých podmienok. Vyžaduje si presýtený priestor parami a súčasné schladenie. Teplota, pri ktorej para skondenzuje, sa nazýva rosný bod a závisí od tlaku a stupňa nasýtenia priestoru parou.
Topenie a tuhnutie
Topenie je premena pevnej látky na kvapalinu, pričom ide o endotermický proces, ktorý spotrebúva teplo. Tuhnutie je jeho presným opakom - premena kvapaliny na pevnú látku, čo je exotermický proces uvoľňujúci teplo.
Teplota, pri ktorej sa látka topí (teplota topenia), a teplota, pri ktorej tuhne (teplota tuhnutia), sú pre väčšinu látok rovnaké. Niektoré látky sa topia pri nízkych teplotách (napr. ľad, maslo), iné pri veľmi vysokých (napr. železo, meď).
Látky sa topia dvomi odlišnými spôsobmi v závislosti od ich štruktúry:
- Kryštalické látky (napr. ľad, soli, kovy) majú pravidelnú vnútornú štruktúru, ktorú možno znázorniť kryštálovou mriežkou. Môžu mať aj pravidelný vonkajší tvar. Ich topenie na grafe závislosti teploty od tepla vyzerá analogicky ako var - teplota najprv stúpa, potom je konštantná počas topenia a po roztopení opäť stúpa.
- Amorfné (beztvaré) látky (napr. čokoláda, parafín, sklo) nemajú pravidelnú vnútornú štruktúru a správajú sa skôr ako kvapaliny s vysokou viskozitou. Ich teplota topenia nie je presne určená, ale udáva sa v intervale. Pri dodávaní tepla ich teplota neustále stúpa, bez zjavného zlomového bodu na grafe.
Pri tuhnutí kryštalických látok teplota najprv klesá, potom je konštantná pri teplote tuhnutia a po úplnom stuhnutí opäť klesá.
Anomália vody
Väčšina látok sa pri zvýšenej teplote rozpína a pri zníženej sťahuje. Voda sa však správa odlišne. Pri tuhnutí svoj objem zväčšuje, pričom najmenší objem dosahuje pri 4°C. Je to spôsobené neúsporným usporiadaním molekúl vody do šesťuholníkov v dôsledku ich tvaru pri nízkych teplotách. Tento jav nazývaný anomália vody má zásadný význam pre život na Zemi. S rastúcim objemom klesá hustota, preto ľad pláva na vode a vďaka svojim izolačným vlastnostiam chráni spodné vrstvy pred zamrznutím.
Fázový diagram
Vzťahy medzi skupenstvami a podmienkami ich existencie popisuje fázový diagram. Na ňom vodorovná os reprezentuje teplotu a zvislá os tlak. Krivky na diagrame znázorňujú skupenské premeny:
- Krivka topenia: reprezentuje rovnováhu medzi pevnou a kvapalnou fázou.
- Krivka nasýtenej pary (vyparovania): reprezentuje tlak nasýtenej pary pri danej teplote, ktorý je zároveň tlakom potrebným na dosiahnutie varu.
- Sublimačná krivka: reprezentuje rovnováhu medzi pevnou a plynnou fázou.
Všetky tri krivky sa stretávajú v trojnom bode, kde môžu tri fázy existovať súčasne v rovnováhe.
V pravom hornom rohu diagramu sa nachádza kritický bod, definovaný kritickou teplotou a kritickým tlakom. Nad kritickou teplotou už látka nemôže existovať v kvapalnom skupenstve. Prekročením kritickej teploty a tlaku vzniká nadkritická tekutina.
Fázový diagram tiež zobrazuje rôzne alotropické (chemické prvky) alebo polymorfické (chemické zlúčeniny) modifikácie tuhého skupenstva, ktoré sa líšia vnútornou štruktúrou a vlastnosťami. Prechody medzi týmito modifikáciami sú tiež reprezentované krivkami.
Metastabilné stavy
Fázový diagram popisuje najstabilnejšie fázy látky pri daných podmienkach. Nie vždy sa však látka pri zmene podmienok okamžite dostane do najstabilnejšieho stavu. Môže existovať v tzv. metastabilnom stave, ktorý nie je energeticky najvýhodnejší, ale jeho premena do stabilnejšieho stavu je spomalená.
Príkladom je prehriata kvapalina. Voda, najmä v poškodených nádobách (škrabance, nečistoty), preferuje vytváranie bubliniek na nerovnostiach. Ak je povrch nádoby dokonale hladký, môže sa stať, že kvapalina dosiahne teplotu varu, ale nevrie, pretože nemá vhodné miesto na tvorbu bubliniek. Takáto prehriata kvapalina (experimentálne bola voda pri atmosférickom tlaku zahriata až na 200°C!) je nestabilná a môže prudko zovrieť, čo chemici nazývajú utajený var. Opačným javom je podchladená para.
Čo je to podchladená voda? Ako to funguje?
Varenie v hrnci, ktorý je poškriabaný, môže viesť k rýchlejšiemu vareniu práve vďaka týmto nerovnostiam, ktoré slúžia ako zárodky pre bublinky. Tlakový hrniec zase zvyšuje tlak, čím zvyšuje bod varu.